Кислород является важной частью атмосферы и необходим для поддержания жизни на земле. Все основные классы структурных молекул в живых организмах, такие как белки, углеводы и жиры, содержат его, как и основные неорганические соединения, которые включают в себя раковины животных, зубы и кости. Элементарный кислород (O2) вырабатывается цианобактериями, водорослями и растениями в процессе фотосинтеза и используется в клеточном дыхании большинством живых организмов на земле.

Общие сведения
Кислород — это газообразный химический элемент. Он обозначается символом O, имеет атомный номер 8 и атомный вес 15,9994, а его молярная масса 32 г/моль. Формула кислорода О2. Схема электронной конфигурации атома кислорода — 1s 2 2s 2 2p 4. Строение атома кислорода имеет две оболочки, как и все элементы, расположенные во втором периоде.

Он представляет большой интерес, поскольку является важнейшим элементом дыхательных процессов большинства живых клеток и процессов сгорания. Это самый распространённый элемент в земной коре. Почти одна пятая (по объёму) воздуха — это О2. Степень окисления -2.
В нормальных условиях О2 — бесцветный газ без запаха и вкуса. Он конденсируется в светло-голубой жидкости. Это реакционноспособный элемент, который образует оксиды со всеми другими элементами, кроме гелия, неона, аргона и криптона. Он умеренно растворим в воде (30 см3 на 1 л растворяющейся воды) при температуре 20 градусов Цельсия.
История открытия
Что такое воздух? Древние народы глубоко задумывались над этим вопросом. И это не удивительно, когда понимаешь, насколько важен воздух для многих процессов. Объекты не могут гореть без воздуха. Человек не может выжить без воздуха. На самом деле, древние народы думали, что воздух должен быть «элементом». Но они использовали слово «элемент» в несколько ином значении, нежели современные учёные. Для древних людей элемент был чем-то очень важным и основным. Воздух соответствует этому описанию, наряду с огнём, водой и землёй. Впоследствии многие учёные повлияли на открытие такого элемента, как кислород:


- Первым человеком в Западной Европе, который описал «части» воздуха, был итальянский художник и учёный Леонардо да Винчи (1452−1519). Леонардо отметил, что воздух не полностью расходуется, когда в нем что-то сжигается. Поэтому он сказал, что воздух должен состоять из двух частей: одной части, которая расходуется на горение, и одной части, которая не участвует в процессе. В течение многих лет идеи Леонардо были не очень популярны среди учёных. Проблема заключалась в том, что у первых химиков не было хорошего оборудования, как в современных лабораториях. Им было сложно собрать образцы воздуха, а затем изучить его.
- В начале 1700-х химики начали узнавать больше о воздухе, но несколько окольным путём. Например, в 1771 и 1772 годах Карл Вильельм Шееле изучал влияние тепла на ряд соединений. В одном эксперименте он использовал карбонат серебра (Ag 2 CO 3), карбонат ртути (HgCO 3) и нитрат магния (Mg (NO 3) 2). Когда он нагревал эти соединения, он обнаружил, что выделялся газ. Затем он изучил свойства этого газа и обнаружил, что пламя ярко горело в нём. Он также заметил, что животные в нём могут безболезненно находиться. Не зная этого, Шееле открыл кислород.
- Примерно через два года Джозеф Пристли провёл аналогичные эксперименты, нагревая оксид ртути (HgO) в пламени. Соединение распалось, в результате чего образовались жидкая металлическая ртуть и газ. Когда Пристли проверил новый газ, он обнаружил те же свойства и характеристики, что и Шееле. Пристли даже пытался вдохнуть тот газ, получение которого ему удалось осуществить.
- Антуана-Лорана Лавуазье (1743−94) часто называют отцом современной химии. Он получил это звание по ряду причин. Наиболее важной из них является объяснение, которое он открыл для процесса сгорания (горения). До исследования Лавуазье химики считали, что горящий объект выделяет вещество в воздух. Они назвали это вещество флогистоном. Например, когда горело дерево, химики говорили, что флогистон перешёл из дерева в воздух. Лавуазье показал, что эта идея неверна. Когда что-то горит, это на самом деле происходит реакция с кислородом в воздухе. Горение, сказал Лавуазье, — это просто окисление (процесс, при котором какое-либо вещество соединяется с О2). Это открытие дало химикам совершенно новый взгляд на химические изменения. Теория флогистона постепенно начала вымирать. Начали развитие многие идеи, которые сегодня используются в современной химии.
Некоторые люди думают, что Шееле следует отдать должное за открытие кислорода. Он завершил свои эксперименты раньше, чем Пристли. Но его издатель очень медленно печатал отчёты учёного. Они действительно вышли после отчётов Пристли. Таким образом, большинство историков сходится во мнении, что Шееле и Пристли должны разделить между собой право на открытие кислорода.
Ни Шееле, ни Пристли до конца не понимали важность их открытия. Этот шаг был предпринят французским химиком Антуаном-Лораном Лавуазье (1743−94). Лавуазье был первым человеком, который объявил, что новый газ является элементом. Он был также первым человеком, который объяснил, как кислород участвует в горении. Кроме того, он предложил название для газа.
Слово oxygenium («кислород») происходит от греческих слов, обозначающих «рождающий кислоту». Лавуазье выбрал такое название, потому что думал, что все кислоты содержат О2. Поэтому новый элемент отвечал за «образование кислот». Однако в этом отношении Лавуазье ошибся. Не все кислоты содержат кислород.
Элемент в окружающей среде
Земная кора состоит в основном из кремниево-кислородных минералов, и многие другие элементы присутствуют в виде их оксидов. Газообразный кислород составляет пятую часть атмосферы. О2 в атмосфере Земли образуется в результате фотосинтеза растений, он накапливался в течение длительного времени, поскольку они использовали обильные запасы углекислого газа в ранней атмосфере и выделяли кислород.
Элемент хорошо растворяется в воде, что делает возможной жизнь в реках, озёрах и океанах. Вода в этих водоёмах должна регулярно снабжаться кислородом, поскольку, когда запасы О2 в ней истощаются, она больше не может поддерживать рыбу и другие водные организмы.

Почти все химические вещества, кроме инертных газов, связываются с кислородом с образованием соединений. Вода, H2O и кремнезём, SiO2, основной компонент песка, являются одними из наиболее распространённых двойных кислородных соединений. Среди соединений, которые содержат более двух элементов, наиболее распространёнными являются силикаты, которые образуют большинство пород и почв. Другими соединениями, которые в изобилии встречаются в природе, являются карбонат кальция (известняк и мрамор), сульфат кальция (гипс), оксид алюминия (боксит) и различные оксиды железа, которые используются в качестве источника металла.
Элемент встречается во всех видах минералов. Некоторые общие примеры включают оксиды, карбонаты, нитраты, сульфаты и фосфаты. Оксиды — это химические соединения, которые содержат кислород и ещё один элемент. Карбонаты — это соединения, которые содержат кислород, углерод и ещё один элемент. В качестве примера можно привести карбонат натрия или соду, кальцинированную соду или солевую соду (Na2CO3), которая часто встречается в моющих и чистящих средствах.
Нитраты, сульфаты и фосфаты также содержат кислород. Другими элементами в этих соединениях являются азот, сера или фосфор плюс ещё один элемент. Примерами этих соединений являются нитрат калия или селитра (KNO3), сульфат магния или соли Эпсома (MgSO4) и фосфат кальция (Ca3 (PO 4)2).
Изотопы кислорода
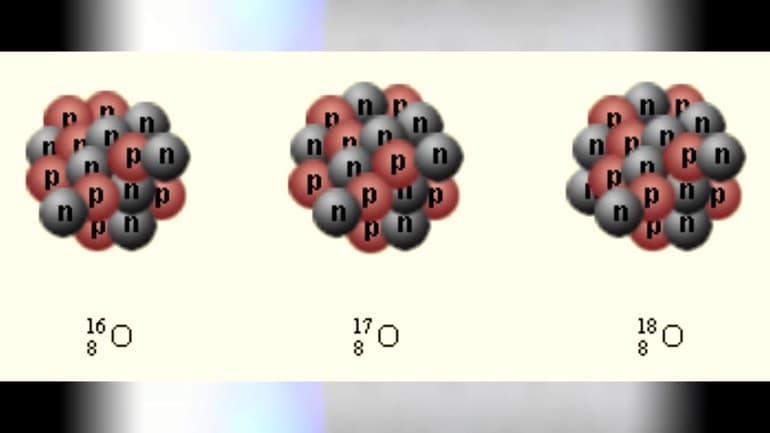
Есть три естественных изотопа О2: кислород-16, кислород-17 и кислород-18. Изотопы — это две или более формы элемента. Они отличаются друг от друга по их массовому числу. Число, написанное справа от названия элемента, является массовым числом. Оно представляет количество протонов плюс нейтронов в ядре атома элемента. Количество протонов определяет элемент, но количество нейтронов в атоме любого одного элемента может варьироваться. Каждая вариация является изотопом.
Известно также пять радиоактивных изотопов элемента. Радиоактивный изотоп — это тот, который распадается на части и испускает некоторую форму радиации. Радиоактивные изотопы образуются, когда очень маленькие частицы обжигают атомы. Эти частицы прилипают к атомам и делают их радиоактивными.
Воздействие на здоровье
Кислород необходим для всех форм жизни, так как он является составной частью ДНК и почти всех других биологически важных соединений. В лёгких этот элемент поглощается атомом железа в центре гемоглобина в крови и, таким образом, транспортируется туда, где он необходим.

Каждый человек нуждается в этом элементе, чтобы дышать, но, как и во многих случаях, слишком большое его количество вредно. Если человек подвергается воздействию большого количества О2 в течение длительного времени, может произойти повреждение лёгких. Вдыхание 50−100% кислорода при нормальном давлении в течение длительного периода приводит к повреждению лёгких. Люди, которые работают с частым или потенциально высоким воздействием чистого элемента, должны пройти тесты на функционирование лёгких до начала работы и по завершении.
Химические свойства
При стандартной температуре и давлении два атома элемента связываются, образуя диоксид кислорода, двухатомный газ без цвета, запаха и вкуса, с формулой O2. Этот элемент является членом группы халькогенов в периодической таблице Менделеева и является высокореактивным неметаллическим элементом. Он легко образует соединения (в частности, оксиды) почти со всеми другими элементами.
Кислород является сильным окислителем и обладает второй по величине электроотрицательностью среди всех реактивных элементов, уступая только фтору. По массе кислород является третьим по распространённости элементом во вселенной после водорода и гелия и наиболее распространённым по массе элементом в земной коре, составляя почти половину массы земной коры. Свободный кислород химически реактивен, чтобы появляться на Земле без фотосинтетического действия живых организмов, которые используют энергию солнечного света для производства элементарного кислорода из воды.
Элементарный O2 начал накапливаться в атмосфере только после эволюционного появления фотосинтезирующих организмов, примерно 2,5 миллиарда лет назад. Двухатомный газообразный кислород в настоящее время составляет 20,8% от объёма воздуха.
Наиболее важными химическими свойствами кислорода являются:

- Поддержание горения. Он помогает другим объектам гореть. Сжигание древесного угля является примером. Древесный уголь — практически чистый углерод.
- Соединяется с элементами при комнатной температуре. Ржавчина является примером. Ржавчина — это процесс, при котором металл соединяется с О2.
- Реагирует со многими соединениями. Распад — это процесс, благодаря которому некогда живое вещество соединяется с кислородом. Продуктами распада являются в основном диоксид углерода (CO2) и вода (H2O):
Сам О2 не горит. Зажжённая спичка в баллоне с чистым элементом горит гораздо ярче, но кислород не загорается.
Физические свойства
Кислород более растворим в воде, чем азот. Вода содержит приблизительно одну молекулу O2 на каждые две молекулы N2 по сравнению с атмосферным отношением приблизительно от одного до четырёх. Плотность кислорода в газообразном состоянии 1,42897 кг/м3. Другими физическими свойствами элемента являются:

- Газ в нормальном состоянии бесцветный, без запаха и вкуса. Жидкий кислород слегка парамагнитен. Он реактивен и образует оксиды со всеми элементами, кроме гелия, неона, криптона и аргона. Умеренно растворим в воде.
- Элемент конденсируется при температуре -182,95С, а замерзает при -218,79С. И в жидком, и в твёрдом состоянии является прозрачным веществом светло-голубого цвета.
- Существование элемента в двух аллотропных формах. Аллотропы — это модификации элемента с различными физическими и химическими свойствами. Аллотропы О2 — это двухатомный кислород и озон, или трёхатомный. Озон встречается в довольно больших количествах в особых условиях. Например, необычно большое количество озона находится в верхних слоях атмосферы Земли. Этот озоновый слой важен для жизни на планете. Он защищает от вредного излучения, которое исходит от Солнца. Озон на уровне земли бесполезен для жизни и может вызвать проблемы со здоровьем у растений, людей и животных.
- Атомарный кислород очень высоко активен. Он способен окислять атомы элементов, которые несвойственны этому организму, и является одним из сильнейших антиоксидантов, который устраняет кислородное голодание тканей и уничтожает практически любую патогенную микрофлору (грибы, вирусы, бактерии и другие) и лишние свободные радикалы.
Применение кислорода
Молекулярный диоксид O2 необходим для клеточного дыхания у всех аэробных организмов. Его реакционноспособные виды, такие как супероксид-ион (O2-) и пероксид водорода (H2O2), являются опасными побочными продуктами использования кислорода в организмах. Однако части иммунной системы высших организмов используют реактивный пероксид, супероксид и синглетный кислород для уничтожения вторгающихся микробов. Реактивные виды также играют важную роль в гиперчувствительной реакции растений на воздействие патогенных микроорганизмов.
В состоянии покоя взрослый человек вдыхает от 1,8 до 2,4 г кислорода в минуту. Это составляет более 6 миллиардов тонн элемента, вдыхаемого человечеством в год. Сферы использования включают в себя следующие:

- Люди, у которых есть проблемы с дыханием, используют кислородные маски и резервуары, чтобы получить необходимый им кислород.
- Он используется в ракетном топливе, сочетается с водородом в двигателе. Когда водород и кислород объединяются, они выделяют очень большое количество энергии. Энергия используется для запуска ракеты в космос.
- На производство металла приходится самый большой процент использования О2. Например, элемент используется для сжигания углерода и других примесей, которые содержатся в железе для производства стали. Небольшое количество этих примесей может быть полезным для стали, но слишком большое делает его ломким и непригодным для использования. Углерод и другие примеси сжигаются при производстве стали путём продувки О2 через расплавленное железо.
- Используется при производстве таких металлов, как медь, свинец и цинк. Эти металлы встречаются в земле в форме сульфидов, таких как сульфид меди (CuS), сульфид свинца (PbS) и сульфид цинка (ZnS). Первым шагом в извлечении этих металлов является превращение их в оксиды. Затем оксиды нагревают с углеродом, чтобы получить чистые металлы.
- Применяется в химической промышленности в качестве исходного материала для производства некоторых очень важных соединений. Иногда этапы перехода от кислорода к конечному соединению являются длительными. Например, газообразный этилен (C2H4) может быть обработан кислородом с образованием этиленоксида (CH2CH2O). Около 60% полученного этиленоксида превращается в этиленгликоль (CH2CH2 (OH)2). Этиленгликоль используется в качестве антифриза и служит отправной точкой при производстве полиэфирных волокон, плёнки, пластиковых контейнеров, пакетов и упаковочных материалов
- Используется в оксиацетиленовой сварке, в качестве окислителя для ракетного топлива, а также в производстве метанола и этиленоксида.
- Растения и животные используют его для дыхания.
- Чистый кислород часто используется для облегчения дыхания у пациентов с респираторными заболеваниями.
Кислород и его соединения играют ключевую роль во многих важных процессах жизни и промышленности
