В области органической химии алкены, также известные как олефины, представляют собой ненасыщенный углеводород. Они состоят из двух атомов углерода и водорода и имеют одну или несколько двойных связей в своей химической структуре, то есть являются непредельными. Гомологический ряд представлен формулой CnH2n. Примеры: С2Н4 — этилен, С3Н6 — пропилен.
Структура и свойства
Структурную (пространственную) изомерию имеют представители с четырьмя и более углеродными атомами. Это означает, что для каждой молекулярной формулы можно создать два и более изомера. Наглядно строение можно увидеть на примере бутена — С4Н8 (СН2 = СН-СН2-СН3):
Однако существует другой вид изомерии — геометрическая. Поскольку углеродная связь не позволяет вращаться вокруг неё, группы СН3 блокируются на одной стороне молекулы или напротив друг друга.
Соединения содержат двойную карбоновую связь. Именно она определяет и меняет физические свойства алкенов:

| Соединения | Точка плавления, ° С | Точка кипения, ° С |
|---|---|---|
| Этилен | — 169 | — 104 |
| Пропен | — 185 | — 47 |
| 1-пентен | — 165 | 30 |
| 1-гептен | — 119 | 115 |
Почти все представители семейства не проводят электричество. Некоторые соединения имеют запах. Например, этилен — сладковатый. А этан совсем не пахнет.
Реакционная способность
Алкеновые соединения относительно стабильные. Однако они более реакционноспособны, чем алканы. Это связано, вероятно, с особенностями связи углерод-углерод. Основные химические свойства алкенов — участие в реакциях.
Первая — реакция добавления. Она происходит путём раскрытия двойной связи. Основной механизм — электрофильное присоединение. Например, гидрогалогенирование, галогенирование, образование галогидрина, оксимеркурация, гидроборирование, добавление дихлоркарбена, реакция Симмонса-Смита, каталитическое гидрирование, эпоксидирование, радикальная полимеризация и гидроксилирование. Более подробно о самых распространённых:


Вторая распространённая химическая реакция — полимеризация. Она даёт полимеры высокой промышленной ценности при большой экономичности процесса. Получаются, например, различные пластмассы, полиэтилен и полипропилен. Полимеры из алкеновых мономеров принято называть полиолефинами или в редких случаях полиалкенами.
Помимо перечисленных, алкены могут участвовать в других реакциях, например, в алкилировании, поэтому часто служат сырьём для нефтехимической промышленности.
Получение алкенов
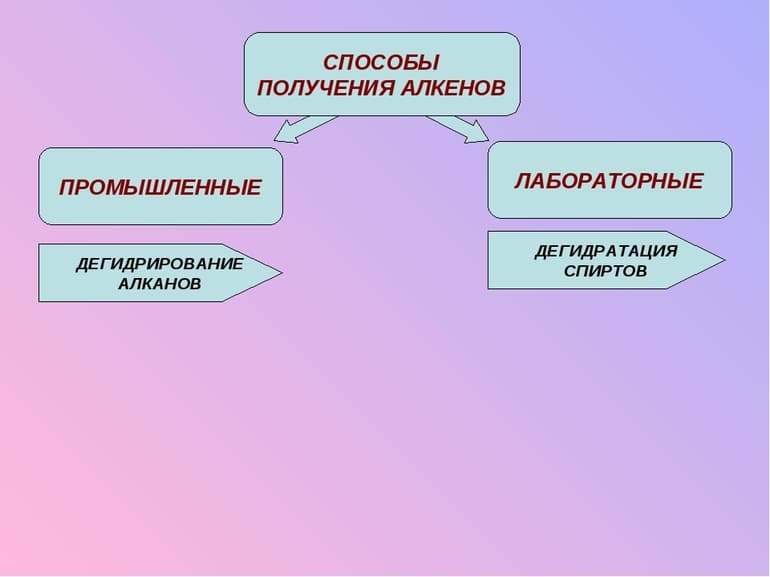
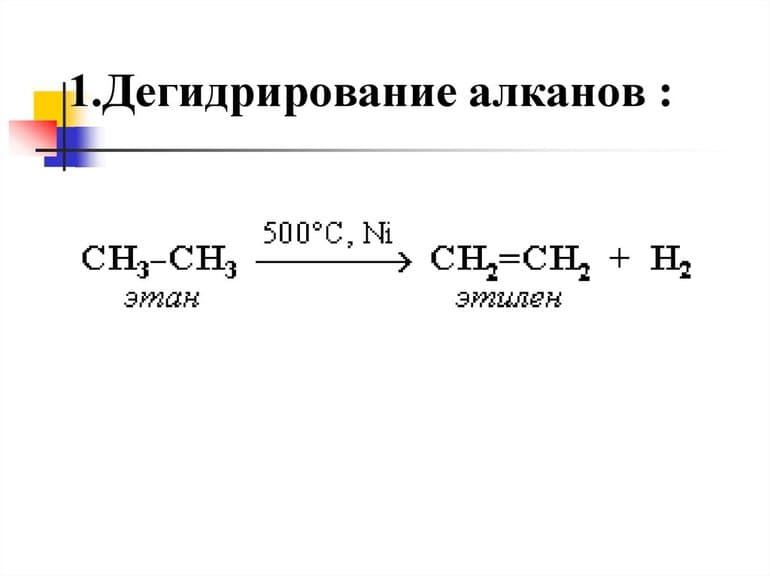
В промцелях алкены получают путём крекинга (сложные молекулы разбиваются на более простые) углеводородов. Основным сырьём являются компоненты природного газового конденсата — этан и пропан. Алканы распадаются при высоких температурах в присутствии цеолитного катализатора. Смесь затем разделяется путём фракционной перегонки. Такой метод используется в основном для получения небольших алкенов, содержащих до шести атомов углерода.
Одним из основных способов синтеза алкенов в лабораторных условиях является удаление в помещении алкилгалогенидов, спиртов и подобных соединений. Самой распространённой считается бета-элиминация по механизму Е2 или Е1. Ещё один метод получения алкеновых соединений включает построение новой углерод-углеродной связи путём сочетания карбонильного соединения (альдегид или кетон) с карбанионным эквивалентом. Такие реакции иногда называют олифенациями. Наиболее известным из этих методов является реакция Виттига.
Алкены могут быть получены путём обмена с другими алкеновыми соединениями в реакции, известной как метатезис олефина. Катализируемое переходным металлом гидровинилирование является ещё одним важным процессом синтеза. Как правило, это включает добавление водорода и винильной группы (или алкенильной) через двойную связь. В настоящее время такую реакцию проводят с помощью таких катализаторов, как железо, кобальт и палладий.
Монозамещённые алкены получают путём карбометаллирования алкинов, что приводит к разнообразию получаемых соединений. Помимо метасинтеза олефинов, используют большое количество перициклических реакций, например, перегруппировку Куопа.
Образование названий
Молекулярная формула углеводорода показывает информацию о возможных типах структур, которые он может представлять. Соединения могут иметь тройную связь, две двойные, одно или два кольца. Поэтому, как и в случае алканов, было необходимо принять последовательную систему номенклатуры, которая могла бы разделять природу этих ненасыщенных химических веществ.
Самыми простыми являются алкены, представляющие собой углеводороды, которые имеют функциональные группы углерод-углеродная двойная связь с формулой CnH2n. Общие правила Международного союза теоретической и прикладной химии (англ. аббр. ИЮПАК) по номенклатуре для класса алкенов гласят:
- На группу указывает суффикс (окончание) -ен.
- Самая длинная цепь, выбранная для имени корня, должна включать оба атома углерода двойной цепи.
- Корневая цепочка должна быть пронумерована от конца ближайшего к атому углерода двойной связи. Если связь находится в центре цепи, для определения конца, где начинается нумерация, используется правило ближайшего заместителя.
- Меньшее из двух чисел, обозначающих атомы углеродной связи, используется в качестве её локатора.
- Соединения называются диеновыми, триеновыми. Добавляется другой эквивалентный префикс, указывающих на количество связей, с присвоением номера локатора.
- Заместителями являются: винильная — Н2С = СН и аллильная группы — Н2С = СН-СН2.
Системные имена алкенов по первому правилу МСТПХ можно представить в виде таблицы. Она содержит первые двадцать представителей с прямой цепью.
| Название | Формула | Название | Формула |
|---|---|---|---|
| Этилен | С2Н4 | Ундецен | С11Н22 |
| Пропен | С3Н6 | Додецен | С12Н24 |
| Бутен | С4Н8 | Тридецен | С13Н26 |
| Пентен | С5Н10 | Тетрадецен | С14Н28 |
| Гексен | С6Н12 | Пентадецен | С15Н30 |
| Гептен | С7Н14 | Гексадецен | С16Н32 |
| Октен | С8Н16 | Гептадецен | С17Н34 |
| Нонен | С9Н18 | Октадецен | С18Н36 |
| Децен | С10Н20 | Нонадецен | С19Н38 |
Согласно второму правилу, если алкен содержит только одну двойную карбоновую связь, и она является концевой, то никаких чисел перед именем не ставят. Например:
- бутан С4Н10 (СН3СН2СН2СН3);
- бутен С4Н8 (СН2 = СНСН2СН3).
В ином случае атомы углерода должны быть пронумерованы таким образом, чтобы дать первому из двух двойных минимально возможное число. При этом оно должно предшествовать суффиксу -ен с тире, например:
- пент-2-ен (СН3СН = СНСН2СН3) — правильно, но допускается написание 2-пентен;
- пент-3-ен (СН3СН2СН = СНСН3) — неверно, поскольку переворот формулы приводит к меньшему числу.
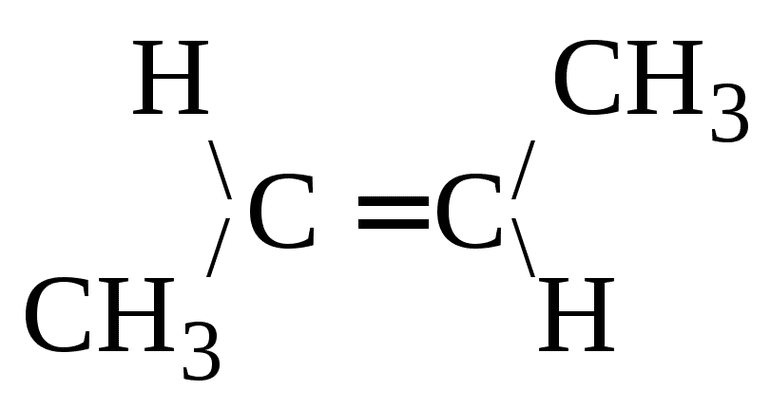
Часто вызывает затруднения шестое правило. Нужно помнить, что общее название этенила — винил, а 2-пропенила — аллил. Формулы заместителей следующие:
- винильный Н2С = СН-;
- аллильный Н2С = СН-СН2 -.
Понять и закрепить правило помогут уравнения. Необходимо взять молекулярную формулу алкена и назвать его, согласно правилам МСТПХ и, наоборот, по имени соединения написать формулу.
Способы применения

В природе алкеновые соединения чаще всего являются частью других веществ. Терпены — основные компоненты эфирных масел. Например, альфа-пинен входит в состав скипидарного масла, а 1-ментен даёт характерный аромат мяте. Конъюгированными полиенами являются, например, витамин А и бета-каротин. В этом контексте интересно отметить, что процесс зрения основан на индуцированной светом цис-транс-изомеризации, связанного с белком ретинола.
Натуральный каучук — полиен, полученный из молочного сока каучукового дерева. Формально этот ненасыщенный углеводород получают путём полимеризации изопрена. Этен — самый простой алкен, также встречается в природе. Как растительный гормон он влияет на созревание плодов. Фрукты, например, киви, которым предстоит долгое путешествие и длительное хранение, собирают рано и держат при низких температурах и высоких СО2 концентрациях. Впоследствии их созревание начинается с обработки плодов газообразным этиленом.
Благодаря качественным характеристикам применение алкенов в промышленной среде довольно разнообразно. Они используются для исходных материалов при синтезе спиртов, пластмасс, лаков, моющих средств и топлива:
К слову, алкены используют для производства ядовитого газа иприта, который является боевым оружием. В быту алкеновые соединения в чистом виде не применяются.
