С диффузией человек сталкивается постоянно. Она обеспечивает дыхание млекопитающих, позволяет чувствовать запахи на больших расстояниях и применяется в различных сферах деятельности, но она может также нести угрозу при загрязнении воздуха опасными веществами. Поэтому важно понимать ее причины и механизмы действия.

Причины
Дадим определение: диффузия в газах – процесс, в ходе которого молекулы и атомы одного газа перемешиваются с молекулами и атомами другого вещества. Для простейшего эксперимента, демонстрирующего диффузию, понадобятся духи или освежитель воздуха. Если побрызгать их в одной половине комнаты, то запах со временем распространится по второй половине.
Происходит это по той причине, что газы, как и другие тела, состоят из молекул, пребывающих в постоянном хаотическом движении. Причем диффузия тем быстрее, чем выше скорость движения молекул. Поэтому, например, запах, исходящий от горячей еды, способен разноситься по всей квартире.
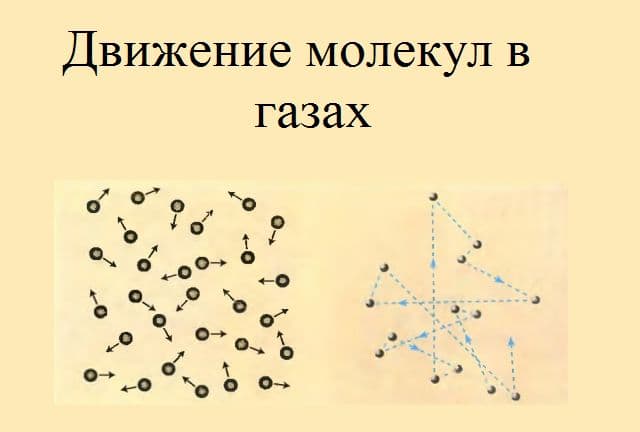
Рис. 1. Движение молекул в газах.
Направление диффузии определяется правилом – компонент смеси стремится заполнить ту часть пространства, где его концентрация меньше. Таким образом, система возвращается к равновесному однородному состоянию.

Рис. 2. Диффузия в газах.
Основной закон диффузии
Для того, чтобы описать диффузию на математическом языке, рассмотрим перенос идеального газа вдоль некоторого направления x через поверхность S, перпендикулярную этому направлению. Масса газа, перенесенная через поверхность за время t, выражается следующей формулой:
$m = – D cdot S cdot t cdot frac{dp}{dx}$, где $frac{dp}{dx}$ – скорость изменения плотность вдоль q, а D – коэффициент диффузии. Знак минус указывает на то, что массоперенос происходит в направлении уменьшения концентрации.
Приведенное выражение называется законом Фика.
Словесная формулировка закона: при наличии разности концентрации газа в разных участках объема возникает диффузионный поток, который приводит к уменьшению разности.
Чаще всего его записывают в дифференциальной форме:
$j = – D cdot gradn_0$, где j – поток газа (или диффузионный поток), $n_0$ – начальная его концентрация, а grad – градиент, дифференциальный оператор, который описывает изменение скалярной величины в малом объеме. В декартовых прямоугольных координатах градиент величины f определяется выражением: $grad f= frac{partial f}{partial x} vec i+ frac{partial f}{partial y} vec j + frac{partial f}{partial z} vec k$; I, j, k – единичные векторы осей x, y, z. То есть, каждое слагаемое здесь – это скорость изменения величины в одном направлении.
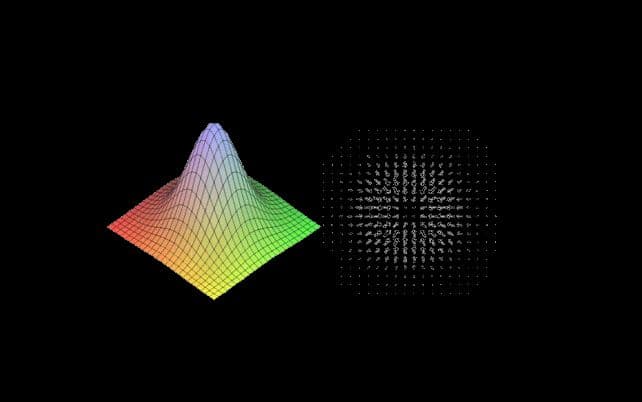
Рис. 3. Графическое изображение градиента.
Коэффициент диффузии рассчитывается по формуле:
$D = frac{1}{3} cdot u cdot lambda$, где $u$ и $lambda$ – средние скорость и пробег молекул газа.
Что мы узнали?
В начале урока, дав определение, рассмотрели бытовые примеры диффузии газов, определили основные закономерности этого процесса, после чего разобрали его математическое описание в законе Фика.
