Огромной популярностью в металлургии и химической промышленности имеет такой физико-химический процесс, как электролиз, происходящий с помощью электролизера. Чтобы понять принцип его действия, нужно изучить определение, нюансы и особенности явления.
Понятие электролиза
Электролиз — процесс, который возникает при воздействии электрического тока на электролит и заключается в выделении электродами составных частей.

Значение явления заключается в том, что путём воздействия электричества на ионы можно организовывать новые формы, структуры или даже сами вещества. Это позволяет человеку контролировать некоторые процессы, протекающие на молекулярном уровне. Законы данного явления в химии и физике открыл английский учёный Фарадей.
Явление происходит при участии электродов, которые делятся на катод и анод:
-
катод — электрод с отрицательным зарядом, на котором происходит восстановление катионов;
-
анод — электрод с положительным зарядом, где происходит окисление анионов.
Приборы чаще всего изготавливаются из материалов, пропускающих электрический ток, например, из графита или большинства металлов. Оба прибора подключаются к отрицательному и положительному полюсам соответственно.
Явление происходит в следующем порядке:
Диссоциация.
Электролиз.
Очень важно не путать такие близкие определения, как гидролиз и электролиз. Первым явлением считается разложение раствора вещества на ионы (заряженные частицы) в воде.
Первый закон Фарадея
Установленный Фарадеем первый закон говорит о прямой пропорциональности между массой вещества, выделившейся в ходе электролиза, и величиной заряда, который прошел через электролит.

Правило подкреплено формулой m = k * q, то есть произведение заряда вещества на его электрохимический эквивалент, что равняется его массе.
Проверка первого закона Фарадея происходит следующим образом:
-
нужно взять три любых электролита, например, А, Б и В и пропустить ток через каждый;
-
если вещества одни и те же, то массы выделившихся можно назвать Г, Г1 и Г2;
-
при этом будет верным следующее равенство: Г= Г1+Г2.
Второй закон Фарадея
Данное правило, установленное Фарадеем, указывает на зависимость между атомной массой вещества, количеством возможных химических связей и самим электрохимическим эквивалентом.

Таким образом, электрохимический эквивалент прямо пропорционален атомной массе вещества, но валентности вещества он обратно пропорционален.
Таблица изменения веществ с помощью электролиза
Усиление восстановительных способностей веществ:
|
Na+ |
Mg2+ |
Al3+ |
Zn2+ |
Fe3+ |
Ni2+ |
Sn2+ |
Pb2+ |
H+ |
Cu2 |
Ag+ |
|
Натрий |
Магний |
Алюминий |
Цинк |
Железо |
Никель |
Олово |
Свинец |
Водород |
Медь |
Серебро |
Усиление окислительных способностей веществ:
|
I- |
Br- |
Cl- |
OH- |
NO3- |
CO32- |
SO42-. |
|
Йодид (соли, образованные йодоводородной кислотой) |
Бромид (соли, образованные бромоводородной кислотой) |
Хлорид (соли, образованные соляной кислотой) |
Гидроксид |
Нитрат (соли, образованные азотной кислотой) |
Карбонат (соли, образованные угольной кислотой) |
Сульфат (соли, образованные серной кислотой) |
|
Катод (отрицательный) |
Анод (положительный) |
|
Восстановление катионов после водорода |
Окисление анионов кислот, не содержащих кислорода |
|
Восстановление катионов, имеющих среднюю активность |
Окисление анионов оксокислот |
|
Восстановление наиболее активных катионов |
Окисление анионов гидроксидов |
|
Восстановление катионов водорода |
|
Уравнения и схемы процессов электролиза, протекающих на катоде и аноде
Электролиз воды
Вода является слабым электролитом, из-за чего процесс будет протекать очень медленно.
Общее уравнение реакции: 2H2O => 2H2 + O2.
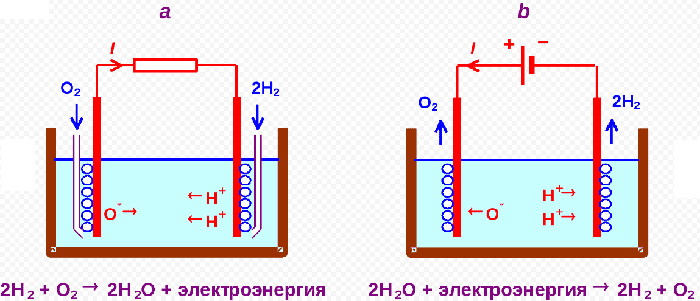
Схема водного электролиза:
|
Анод |
Катод |
|
2H2O => O2 + 4H+ + 4e– |
4H+ + 4e– => 2H2 |
|
3H2O => O3 + 6e– + 6H+ |
O2 + 2H2O + 2e– => H2O2 + 2OH– |
Электролиз расплавов солей
Данную разновидность реакции можно рассмотреть на примере расплава гидроксида натрия, то есть NaOH.

|
Диссоциация гидроксида |
NaOH => Na+ + OH- |
|
Окислительный и восстановительный процессы |
4OH- — 4ē => 2H2O + O2↑ (окисление) Na+ + 1ē => Na0 (восстановление) |
|
Электролиз |
4NaOH => 4Na + 2H2O + O2↑ |
Электролиз растворов солей
Явление можно рассмотреть на примере поваренной соли, имеющей формулу NaCl.

Схема с использованием инертных электродов:
|
Диссоциация соли |
NaCl => Na+ + Cl- |
|
Окислительный и восстановительный процессы |
2Cl- — 2ē => Cl2↑ 2H2O + 2ē => H2↑ + 2OH-. |
|
Электролиз |
2NaCl + 2H2O => H2↑ + Cl2↑ + 2NaOH. |
Таким образом, продуктом химической реакции было получение гидроксид натрия.
Также следует отметить такую особенность солей карбоновых кислот, как их способность к декарбоксилированию, как например реакция с ацетатом калия:
2CH3COOK + 2H2O => H2+ 2KOH + CH3-CH3 + 2CO2.
Электролиз веществ — одна из важнейших тем при изучении химии как неорганической, так и органической. Нужно научиться решать подобные задачи для полного понимания химических процессов и метаморфозов веществ.
