Среди классов неорганических веществ особое место занимают оксиды. Это категория соединений, в состав которых входит кислород, имеющий степень окисления -2. Важную часть от указанного класса, занимают кислотные оксиды.
Общая характеристика
Это солеобразующие соединения, то есть в результате химической реакции они образуют соль. В состав, помимо кислорода, могут входить:
- неметаллы (CO₂, P₂O₅);
- металлы 4-6 групп побочных подгрупп в наивысшей степени окисления (Mn₂O₇, MoO₃).
По агрегатному состоянию они могут быть газами (SO₂, CO₂), жидкостями (SO₃), твердыми веществами (P₂O₅).
Способы получения оксидов
Горение простых и сложных веществ: 4P + 5O₂ = 2P₂O₅; CH₄ + 2O₂ = CO₂ + 2H₂O Разложение при нагревании ряда сложных химических соединений: t СaCO₃ → CaO + CO₂ Выделение кислот из воды (как побочный продукт): 2HNO₃ + P₂O₅ = 2HPO₃ + N₂O₅
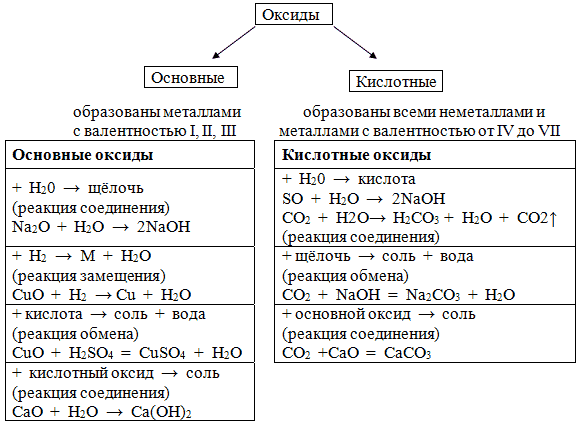
Рис. 1. Классификация оксидов
Химические свойства
Свойства рассматриваемого класса связаны с его способностью к реакциям с различными классами неорганических веществ:
- взаимодействию с водой:
СrO₃ + H₂O = H₂CrO₄
- взаимодействию с гидроксидами:
3Ca(OH)₂ + P₂O₅ = Ca₃(PO₄)₂ + 3H₂O
- реакциям с основными оксидами:
СO₂ + CaO = CaCO₃
- реакциям с амфотерными оксидами:
P₂O₅ + Al₂O₃ = 2AlPO₄
Основные представители
- Углекислый газ (СO₂). Не имеет цвета и запаха, растворим в воде, тяжелее воздуха. Образуется в результате процессов гниения или горения органических продуктов. С известковой или баритовой водой дает характерное помутнение, что позволяет его обнаружить.
- Сернистый газ (SO₂). Не имеет цвета, с характерным запахом, хорошо растворим в воде. При взаимодействии с сильными окислителями (бромной водой или перманганатом калия) происходит обесцвечивание последних, что является качественной реакцией и позволяет обнаружить сернистый газ.
- Оксид марганца (VII) — Mn₂O₇. Зелено-бурое маслянистое вещество, сильный окислитель, который взрывается при любом ударе. Такие соединения, как спирт, при взаимодействии с ним воспламеняются.
Применение
Рассмотренные кислотные оксиды эффективно используются в химических синтезах. Углекислый газ играет важную роль в процессе фотосинтеза. Еще больше примеров для полного понимания темы смотрите в предложенном ниже видео.
