В 1772 году шведский химик Шееле открыл элемент кислород. Химические свойства этого вещества оказались воистину уникальными: он реагирует практически со всеми металлами (кроме золота и платины), взаимодействует с неметаллами, органическими и неорганическими веществами. Позднее, в 1774 году, это же доказал и английский ученый Пристли.

Нахождение в природе и физические свойства
Кислород (формула O2) — элемент, который наиболее распространен в земной коре (его весовое содержание составляет 49,13%). Также он содержится в воздухе, где его 23%, входит в состав воды (88,9%), во всех оксидах и кислородосодержащих солях. Общая характеристика кислорода при обычных условиях:
- бесцветный газ;
- не имеет запаха;
- плохо растворим в воде (как и в других растворителях);
- сжижается при -183°C, а затвердевает при -219°C.
Примечательно, что в жидком и твердом состоянии O2 приобретает цвет: он становится голубым. А еще он притягивается магнитом.

В таблице периодической системы находится в главной подгруппе (классе) VI группы. Элементы, расположенные здесь, на внешнем электронном слое имеют по 6 электронов, поэтому могут либо присоединять 2 электрона, либо (кроме кислорода) отдавать 4 или 6 электронов. Именно этим и объясняются их физ. и хим. свойства.
При нормальных условиях чистый кислород малоактивен, но в присутствии воды его реакционная способность усиливается. Реакции, которые протекают с участием этого вещества, называются горением. К этому процессу относится и ржавление, а также дыхание (медленное горение).
Примечание: химическая сущность дыхания состоит в соединении углерода и водорода органических веществ с кислородом.
Химические характеристики и соединения
С точки зрения химии, этот элемент — типичный активный неметалл. Во всех соединениях он проявляет степень окисления -2 (исключение — реакции с фтором). Как может протекать взаимодействие веществ с кислородом:
- Уравнения взаимодействия с металлами. 2Ca + O2 → 2CaO (оксид кальция или негашеная известь); 4Al + 3O2 → 2Al2O3.
- Реакции с неметаллами — в результате образуются несолеобразующие оксиды. S+O2 → SO2 (сернистый газ); N2 + O2 → 2NO (окись азота).
Кроме этих веществ, кислород хорошо вступает в реакции с органическими и неорганическими соединениями (с серой, углеродом, сульфидами металлов — то есть с соединениями, которые горючи в атмосфере O2). Со сложными веществами взаимодействие будет протекать по плану (реакции горения):
- CH4 + 2O2 → CO2 + 2H2O.
- 4Fe (OH)2 + O2 + 2H2O → 4Fe (OH)3.
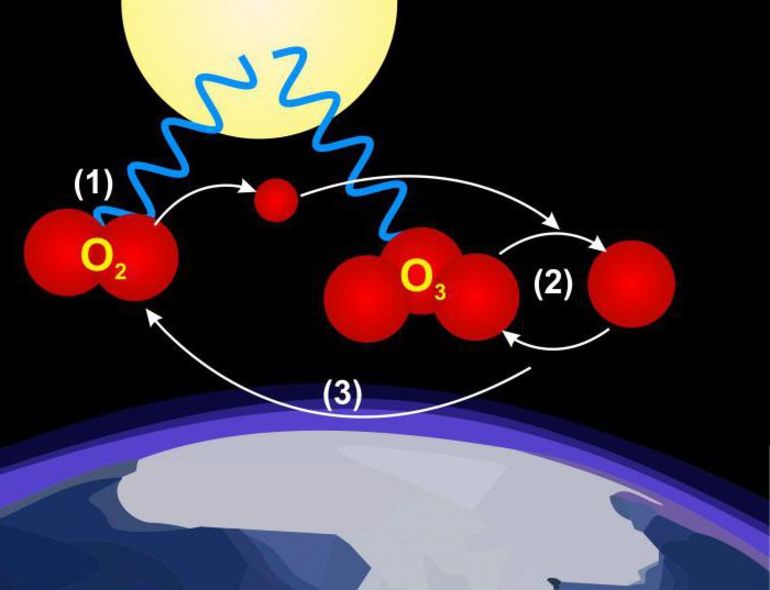
Справка: в атомарном состоянии элемент более активен, чем в молекулярном. Именно на этом свойстве основано применение кислорода в качестве отбеливающего агента — так легче разрушаются окрашивающие органические вещества.
В молекулярном состоянии кислород может существовать в виде O2 и озона O3, то есть для него характерно явление аллотропии (существование нескольких простых веществ одного и того же химического элемента).
Оксиды и пероксиды
Если говорить кратко, можно сказать, что кислород образует два типа соединений: оксиды и пероксиды. При этом первые из названых можно рассматривать как производные воды (схема): H-O-H, Na-O-Na. Вторые же можно охарактеризовать как пероксидов водорода (тоже схематично): H-O-O-H, Na-O-O-Na.
Получить оксиды можно несколькими способами. Первый — это непосредственным взаимодействием с элементами, а второй — разложение при нагревании гидроксидов или солей. Примеры:
- Непосредственное взаимодействие. 2Mg + O2 → 2MgO.
- Разложение. Cu (OH)2 → CuO + H2O; CaCO3 → CaO + CO2.
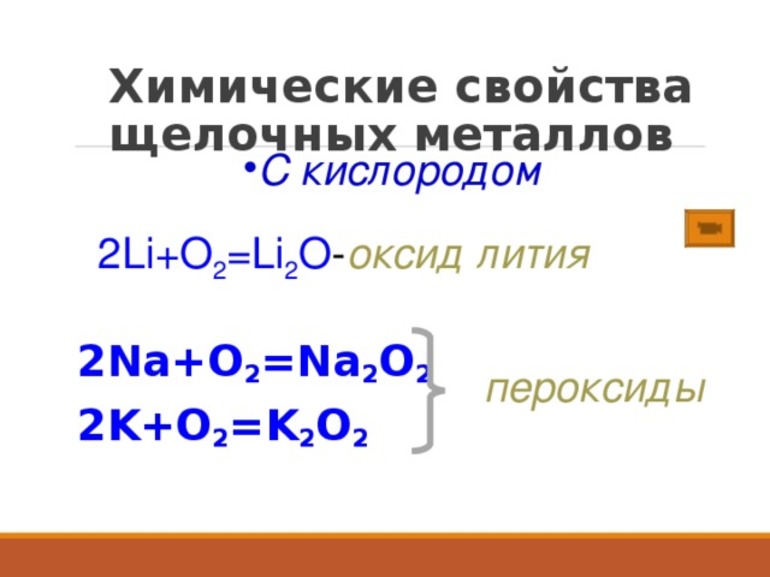
С кислородом не будут прямо соединяться галогены, некоторые газы и благородные металлы. Щелочные металлы, за исключением лития, при взаимодействии будут образовывать пероксиды или супероксиды: 2Na +O2 → Na2O2; K + O2 → KO2 (супероксид).
Ряд окислов может соединяться с водой, образуя гидроксиды кислот — такие будут называться кислотными оксидами или ангидридами. К таким относятся SO2 (сернистый ангидрид), CO2 (угольный ангидрид). Те кислородные соединения, которые с водой образуют основания, именуют основными.
Часть оксидов обладает амфотерными свойствами. Гидроксиды таких соединений могут выступать кислотами или основаниями.
Высшие оксиды металлов (то есть те, где он находится в высшей степени окисления) всегда обладают кислотными свойствами: V2O5, Cr2O3. Известна также группа индифферентных (несолеобразующих) окислов: CO, SiO, NO.
Большинство бинарных кислородных соединений устойчивы к нагреванию. А вот оксиды благородных металлов при повышении температуры легко разлагаются.
Озон (O3) — аллотропная модификация
Это соединение образуется при медленном окислении влажного белого фосфора, а также при разложении концентрированной серной кислоты, перманганата калия, бихромата калия и некоторых других соединений (в этом случае O3 — примесь).

В природе озон образуется при окислении смолы хвойных деревьев, ультрафиолетовом облучении кислорода в верхних слоях атмосферы. Качественная реакция на присутствие O3 в воздухе:
O3 + 2KI + H2SO4 → I2 + K2SO4 + H2O + O2.
В промышленности его получают при действии тихого электрического заряда на O2: 3O2 → 2O3. Реакция протекает в специальном приборе — озонаторе, чистое вещество отделяется сжижением.
По внешнему виду — синяя жидкость, взрывоопасная. От соприкосновения с ним эфиры, спирты, скипидар воспламеняются. Озон разрушает многие органические вещества, а микроорганизмы вообще убивает. Какие химические свойства характерны для него:
- при воздействии на ненасыщенные органические вещества O3 присоединяется к ним по месту двойной связи, в результате чего образуются озониды;
- это сильный окислитель.
Благодаря своим бактерицидным свойствам озон широко применяется в промышленности: в пивоваренном производстве, для обеззараживания воды.
Получение кислорода
Один из методов получения — рефракционная перегонка воздуха, но такой кислород содержит около 3% инертных газов (в основной это аргон). Другой вариант — ректификация жидкого воздуха. Этот процесс можно кратко описать так:
- воздух сжимают при давлении 100−200 атм;
- нагревают, после чего охлаждают в специальных аммиачных холодильниках;
- охлажденную смесь пропускают через дроссель, при выходе из которого давление резко падает.
При расширении газов температура понижается, и воздух сжижается. Эта операция повторяется многократно для увеличения выхода конечного продукта.

Сжиженный воздух — смесь газов (в основном это азот и кислород, остальных там меньше 1%). Из-за разницы температур кипения (у N2 она -195,8°C, кислород закипает при -183°C) из жидкого воздуха отгоняется азот, а затем O2.
Полученный этим методом кислород содержит примеси азота, поэтому его подвергают дополнительной очистке.
В лаборатории его можно получить несколькими способами. Основные из них:
- Разложение бертолетовой соли. Реакция протекает при повышенной температуре и в присутствии катализатора, в роли которого используют диоксид марганца: 2KClO3 → 2KCl + 3O2.
- Процесс разложения перманганата калия при нагревании: 2KMnO4 → K2MnO4 + MnO2 + O2.
- Выделяют из нитратов щелочных металлов: 2NaNO3 → 2NaNO2 + O2.
- В процессе распада оксида ртути: 2HgO → 2Hg + O2.
Еще один способ синтеза — электролизация воды в присутствии гидроксидов щелочных металлов, например, KOH. Эти вещества добавляются для увеличения электропроводности.
Применение и промышленное значение
Благодаря своим свойствам кислород широко применяется в технике. В присутствии этого элемента окислительные процессы протекают гораздо интенсивнее, чем в простом воздухе. При этом повышается температура пламени. Поэтому O2 активно применяется для интенсификации окисления в химической и металлургической промышленности (выплавка чугуна и стали, обжиг сульфидных руд, резка металлов и прочее).

Смеси жидкого кислорода с горючими веществами (углерод, сера, древесные опилки) под названием оксиликвиты используются как взрывчатое вещество в горной и горнодобывающей промышленности (при проведении горно-взрывных работ). Чистый O2 применяется в медицине (при лечении бронхиальной астмы, органов ЖКТ — приготовление специальных коктейлей, и прочее), в кислородных приборах при работе под землей и под водой, на больших высотах. Незаменим он и в процессе производства ракетного топлива (окислитель).
