Стериоизомеры — соединения, одинаковые по своей химической структуре, но отличные по пространственному расположению молекул. Одним из видов стериоизомерии является геометрическая. Второе ее название цис-транс-изомерия. У изомерных молекул этого типа разное расположение радикалов в пространстве. Цис-транс-изомерия характерна для соединений с ненасыщенной (двойной) связью и для молекул, имеющих циклическую структуру.
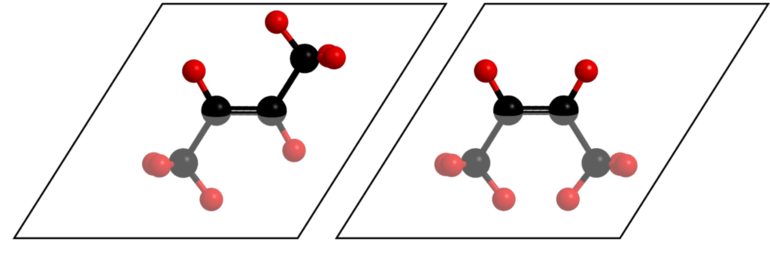
Условия для пространственной изомерии
Не все химические соединения обладают способностью образовывать геометрические изомеры. Пространственная цис-транс-изомерия возможна для следующих веществ:
- алкенов;
- циклоалканов;
- алкадиенов;
- ненасыщенных жирных кислот.
Чтобы молекула могла принимать различные формы в пространстве, должно выполняться 2 условия.
Ненасыщенная или циклическая молекула
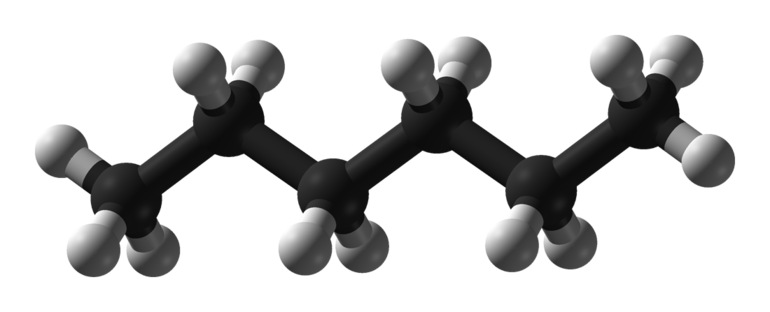
Важным условием для получения структурной изомерии молекул является наличие двойной связи или неароматического кольца. У гексана, как представителя алканов, не будет существовать пространственных изомеров. Так же они не встречаются у алкинов. Например, у атомов углерода в веществе бутин-2 будет только одна метильная группа радикалов, поэтому пространственная изомерия не наблюдается.
При пространственном изображении молекул такого типа плоскость проводят через 2 атома углерода, соединенных двойной связью, или через ароматическое кольцо. Остальные радикалы располагаются в пространстве относительно этой плоскости. Цис-изомер — молекула, у которой одинаковые радикалы лежат на одной стороне от плоскости симметрии. У трансизомера радикалы расположены крест накрест относительно двойной связи.
Например, вещество бутен-2. Это алкен с длиной цепочки в 4 атома углерода. Формула записывается СН3 — СН = СН — СН3. При условном изображении цис-формы, атомы водорода будут расположены вверху от кратной связи, а метильные группы внизу. У транс-бутена расположение заместителей будет симметричным.
Алкадиены — ненасыщенные углеводороды, имеющие 2 двойные связи и не цикличные по своей структуре. Цис- транс-изомеры имеются у веществ из гомологического ряда бутадиена R-CH=CH-CH=CH2. Плоскость симметрии у алкадиенов проходит через одну двойную связь, а заместителями являются группы R- и -CH=CH2. Для ненасыщенных жирных кислот определение цис-транс-изомеров будет аналогичным.
Для циклических соединений пространственная изомерия зависит от расположения заместителей относительно ароматического кольца. В молекуле диметилциклобутана атомы водорода замещают 2 метильных радикала.
У цис — диметилциклобутана замещающие группы расположены по одну сторону от кольца, а атомы водорода по другую. В транс-изомере расположение радикалов будет перекрестным.
Разные заместители
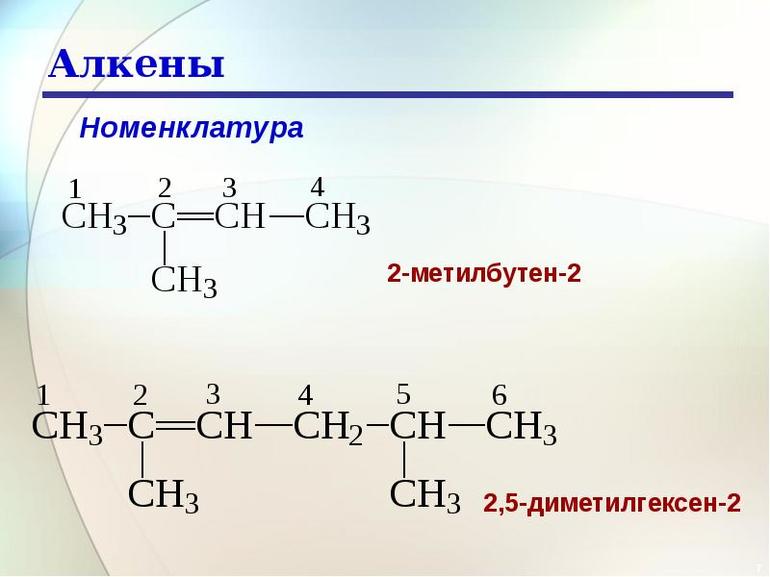
Второе важное условие для существования геометрических форм — наличие разных заместителей при атоме углерода. Например, для бутадиена пространственные формы невозможны, так как при одном из атомов находятся только 2 водорода. Так же 2 — метилбутен — 2 не образует пространственных изомеров, из-за двух радикалов метила при одном атоме углерода. Чтобы существование их стало возможно, необходимо увеличить длину цепочки. Например, октен — 2 образует структурные изомеры, так как при каждом атоме углерода находится водород и алкильный радикал.
Отличие в свойствах
Разная пространственная форма молекул влияет на физические свойства веществ. У различных геометрических форм будут отличаться:
- точка кипения;
- точка плавления;
- растворимость .
Влияние на различие свойств пространственных изомеров оказывает природа функциональных групп и то, какое расстояние между ними. Если заместители представлены слабыми донорами, их влияние на свойства вещества будет несильным. Например, цис — и транс пентен — 2 почти не отличаются по физическим свойствам, потому что водород замещают метильная и этильная группы.
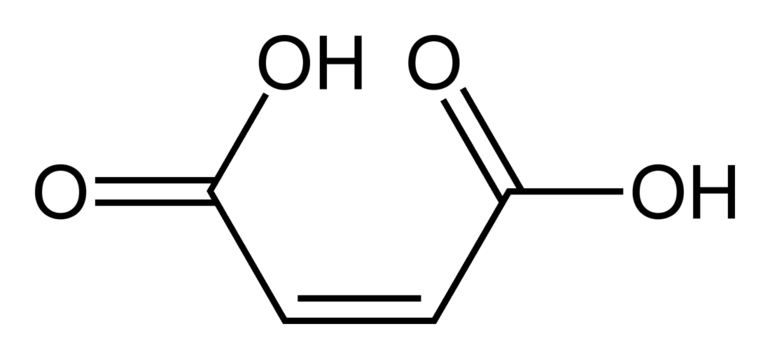
Но если есть полярная группа, влияющая на двойную связь, свойства пространственных форм существенно отличаются. Например, малеиновая кислота по физическим свойствам и химической активности сильно отличается от фумаровой. Но обе они являются изомерными формами бутендиовой кислоты. Это связано с тем, что у цис — изомера расстояние между функциональной группой и радикалом меньше, чем у транс — изомера.
На свойства молекул влияние так же оказывает симметричность. Трансизомеры симметричны, поэтому молекулы расположены очень плотно. Температура плавления из-за этого существенно выше, чем у не симметричных цис — изомеров.
Соотношение изомеров
У молекул простых алкенов высокая энергия вращения относительно кратной связи. Это позволяет отдельно существовать цис— транс— изомерам. Примером алкена служит гексен — 3 СН3 — СН2 — СН= СН — СН2 — СН3.
Однако энергию вращения можно понизить. Для этого в молекулу нужно внести сильный донор по одну сторону от кратной связи, и сильный акцептор — по другую. К таким соединениям относятся амидные производные эфиров и кетонов. Соотношение пространственных изомеров для таких веществ зависит от природы растворителя.
