У производных аммиака с замещенными атомами водорода или аминов химические свойства зависят от замещающих групп. Эти соединения в зависимости от состава могут быть газообразными, жидкими или твердыми. Низшие амины имеют характерный запах протухшей рыбы, высшие не пахнут.
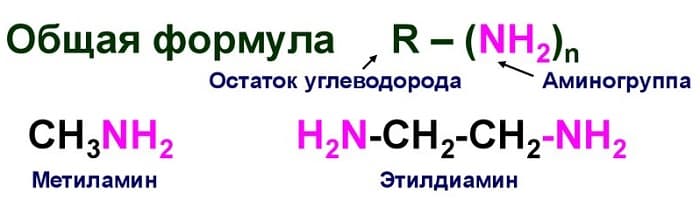
Номенклатура и общая формула
Номенклатурное наименование азотсодержащего органического соединения может образовываться двумя способами:
-
путем добавления к названиям связанных с азотом органических остатков окончания «амин»;
-
добавляя приставку «амин» к наименованию высшего углевода.
Правильно применить правила к наименованию соединения можно, исходя из общей формулы и применимой классификации.

В зависимости от количества замещенных в аммиаке NH₃ углеводородными радикалами атомов водорода, можно выделить следующие типы соединений:
R-NH₂, первичные амины.
R₂-NH, вторичные.
R₃-N, третичные соединения с замещением всех атомов водорода углеводородными радикалами.
Также возможно замещение четвертого атома водорода в катионе аммония, благодаря чему амины способны формировать аналоги солей аммония RH₄⁺.
Примеры номенклатурных наименований:
-
CH3NH₂ — метиламин, первичный тип соединения;
-
(C₂H5)₂NH – диэтиламин, вторичный амин с одинаковыми углеводородными радикалами.
Если углеводородные заместители не совпадают, их перечисляют в алфавитном порядке. Некоторые соединения этого типа больше известны под своими тривиальными названиями, например, фениламин также называют анилином.
Изомерия и структурные формулы аминов
Для производных аммиака с замещенными атомами водорода характерны два основных типа изомерии:
-
структурная изомерия;
-
оптическая изомерия.
Каждый тип структурных изомеров характеризуется низшим амином, начиная с которого он доступен.
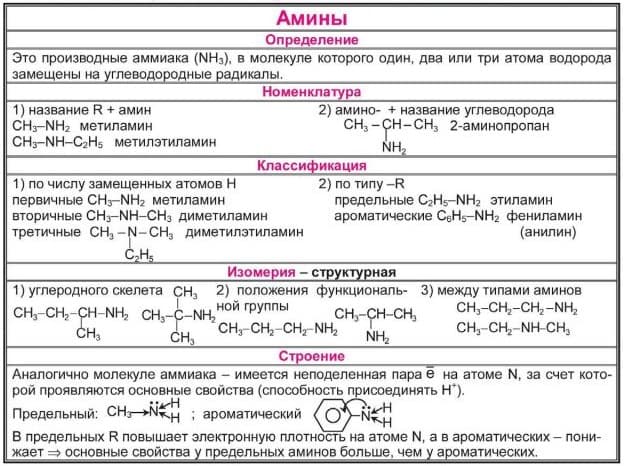
Можно выделить три основных признака структурных изомеров:
-
изомерия углеродного скелета, при которой количество замещенных атомов водорода остается неизменным, но меняется структура углеводородного радикала;
-
положение аминогруппы в углеводной цепочке наблюдаемое, начиная с пропанамина и изопропанамина;
-
изомерия аминогруппы, при которой отличается количество атомов водорода, замещенных углеводородными цепочками.
Строение углеродного скелета изомеров на примере бутанамина:
СН₃-СН₂-СН₂-СН₂-NH₂
бутиламин (бутанамин-1);
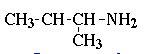
вторбутиламин (бутанамин-2);
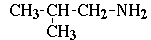
изобутиламин (2-метилпропанамин-1);
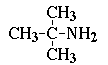
третбутиламин (2-метилпропанамин-2).
Изменение положения аминогруппы в углеводородной цепочке также приводит к появлению изомеров.

Физические свойства
Благодаря полярной связи H-N амины обладают способностью формировать водородные связи, благодаря чему их температура кипения заметно выше, чем у углеводородов с той же длиной цепочки.
По мере увеличения молекулярной массы агрегатное состояние веществ в нормальных условиях меняется от газообразного к твердому. Газообразные метиламин, диметиламин и триметиламин имеют аммиачный запах. Жидкие вещества пахнут протухшей рыбой, твердые амины не пахнут.
Некоторые физические свойства приведены в таблице:
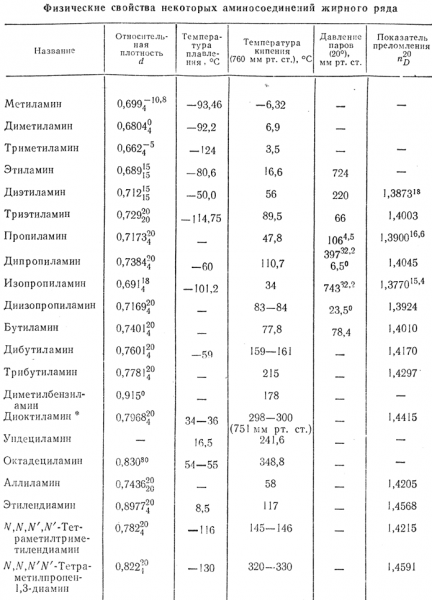
Химические свойства
Способность аминов вступать в химические реакции можно разделить на их поведение в водном растворе, взаимодействие с кислотами и окисление. Аналогичным образом ведут себя другие вещества, содержащие амидную группу, например, аминокислоты (аминоуксусная или глицин, аланин и др.).
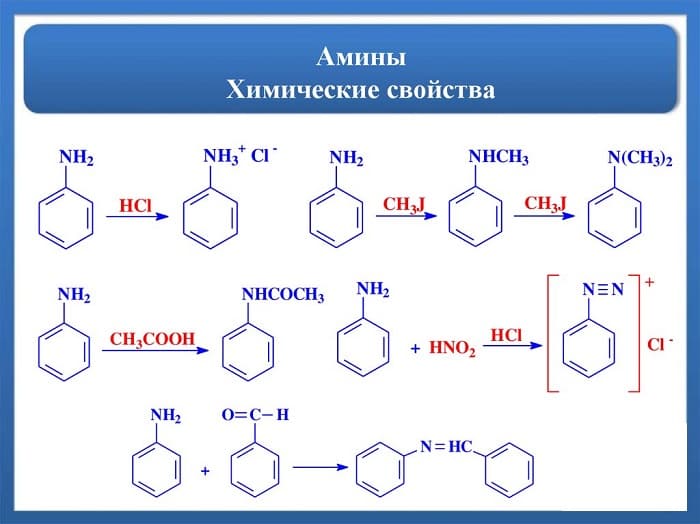
Основные свойства эти вещества проявляют благодаря наличию на атоме азота электронной пары. Сила аминов как оснований относительно аммиака определяется типом углеводородных радикалов в их структуре: алифатические амины сильнее аммиака, а ароматические – слабее. Благодаря донорно-акцепторному взаимодействию с молекулами воды, их растворы имеют щелочную реакцию.
При взаимодействии с кислотами амины образуют нестабильные соли, разлагаемые при добавлении щелочи с выделением чистых аминов.
Реакции взаимодействия диметиламина с серной кислотой и получившегося сульфата метиламмония с выделением газообразного диметиламина:
2CH₃-NH₂ + H₂SO₄ → [CH₃-NH₃]₂SO₄
[CH3-NH3]2SO4 + 2NaOH → 2CH3-NH2 ↑ + Na2SO4
+ H2O
По взаимодействию с азотистой кислотой можно определить, к какому типу – первичному, вторичному или третичному относится реагирующее вещество.
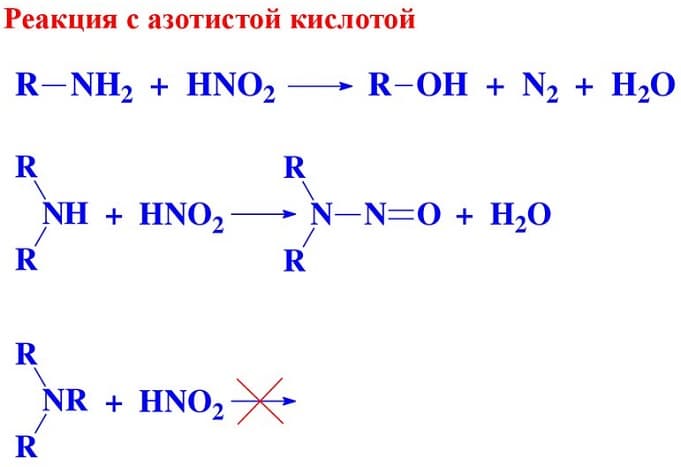
Качественная реакция с НNO2 приводит к образованию:
-
спирта — при реакции с первичным алифатическим амином с выделением азота;
-
ароматического спирта — при соединении с первичным ароматическим амином при комнатной температуре;
-
при реакции со вторичным амином любого типа образуется нитрозоамин — маслянистое желтоватое вещество, содержащее нитрозо-группу -N=O;
-
при соединении с третичными ароматическими аминами образуются кристаллы зеленого цвета пара-нитропроизводных, являющихся результатом реакции замещения по бензольному кольцу.
Единственный тип веществ, не вступающий в реакцию с разбавленной азотистой кислотой при комнатной температуре – третичные алифатические амины. При горении этих соединений образуются вода, азот и углекислый газ.
Ароматические амины взаимодействуют с кислородом воздуха и окисляются, в результате чего темнеют.
Получение аминов
Промышленное получение этих азотсодержащих соединений началось с получения анилина русским химиком-органиком Н. Н. Зининым в 1842 году. Реакция, названная именем известного химика, предусматривает восстановление нитробензола сульфидом аммония по следующему химическому уравнению:
Промышленная схема производства анилина выглядит следующим образом:
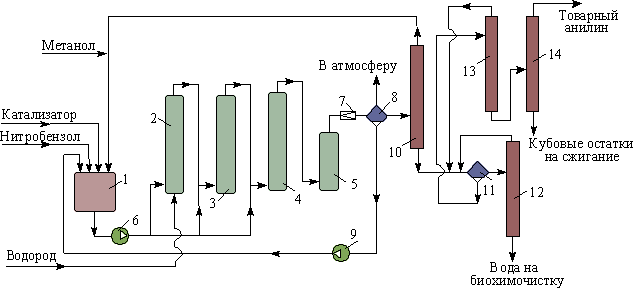
Другие способы получения, используемые на производстве и в лабораторных условия, включают в себя:
-
восстановление амидов алюмогидридом лития;
-
восстановительную реакцию для получения первичных аминов, где в качестве исходного вещества предусматривается нитрил;
-
различные виды реакции алкилирования, при которой в молекулы аммиака или низшего амина вводится алкильная группа.
Применение
Амины широко применяются в промышленности, в основном в качестве сырья.
Известны следующие сферы их использования:
-
в качестве сырья для производства синтетических волокон, таких как нейлон;
-
как исходный компонент при производстве полиуретановых волокон и других видов этого полимера;
-
как основа для изготовления анилиновых красителей;
-
для синтеза средств борьбы с вредителями (фунгицидов, репеллентов, инсектицидов и др.);
-
в качестве катализатора в химической промышленности и металлургии;
-
в фармацевтическом и косметическом производстве.
Веществом, имеющим широкое применение, является анилин, активно использующийся для производства красителей, лекарственных средств различных типов, формальдегидных смол и взрывчатых веществ.
Вредное воздействие аминов
Почти все представители этого класса химических веществ представляют опасность для здоровья. Самый распространенный из них – анилин – обладает ядовитыми парами и легко проникает в организм через кожу. При отравлении этим веществом появляется одышка, посинение губ, учащенное сердцебиение.

Первая помощь предусматривает смыв вредного вещества с кожи, чистый воздух и незамедлительный вызов медпомощи.
Заключение
Подведём итог вышесказанному:
-
химия азотсодержащих органических соединений имеет широкое практическое применение в различных отраслях промышленности;
-
производятся они путем восстановления азотсодержащих соединений;
-
могут быть жидкими, твердыми или газообразным;
-
в растворе имеют щелочную реакцию и вступают в реакцию с кислотами;
-
в большинстве своем ядовиты.
