Структура белка необычайно важна для соединений, так как все функции они выполняют, принимая определённую пространственную конфигурацию.
Белки – это природные полимеры, молекулы которых состоят из остатков аминокислот, соединенных амидными (пептидными) связями.
Мономерами для образования макромолекулы служат α-аминокислоты. Это соединения, содержащие аминогруппу у первого атома углерода, не считая углерод карбоксильной группы.
Таких аминокислот известно 20. Из этого количества создаётся всё многообразие белков. Некоторые аминокислоты могут образовываться в организме, их называют заменимыми. Те, которые поступают только с пищей – незаменимые. В зависимости от состава, белки делят на полноценные, содержащие незаменимые аминокислоты, и неполноценные, не содержащие незаменимые аминокислоты.
Состав, строение и функции белков очень сложные, изучает эти вопросы биология. Рассматриваются природные полимеры и в курсе химии. Состав их можно выразить формулой:
(–HN – CHR – CO –)n
В природные полимеры входят химические элементы: углерод, кислород, водород, азот, сера. В состав некоторых соединений включены фосфор, селен железо, медь и прочие элементы.
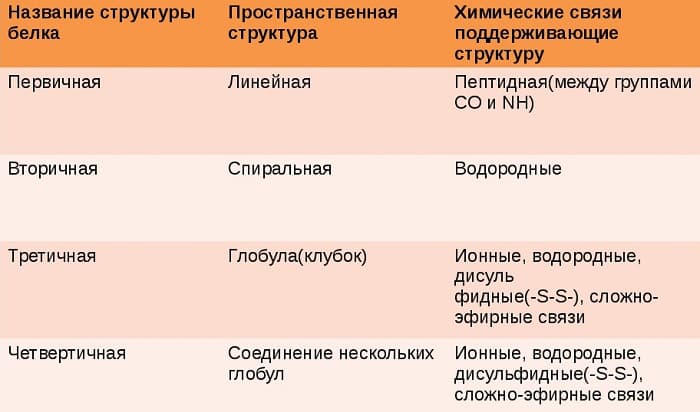
Первичная структура белка
Последовательно соединенные друг с другом аминокислотные остатки в цепь образуют первичную структуру. Цепь образована пептидной химической связью. Этот уровень организации самый важный. Случайная замена одной аминокислоты вызывает тяжелое генетическое заболевание.
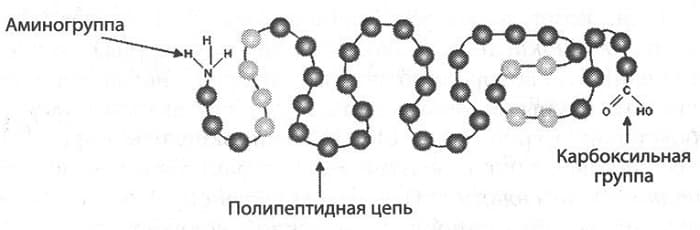
Белковые молекулы образуются в процессе биосинтеза на рибосомах. Здесь реализуется наследственная информация. Последовательность аминокислотных остатков определяется последовательностью нуклеотидов в и-РНК. Зависимость триплетов и аминокислот записана в таблице генетического кода.
Если первичный уровень организации белка задаётся правильно, остальные структуры макромолекула принимает самопроизвольно.
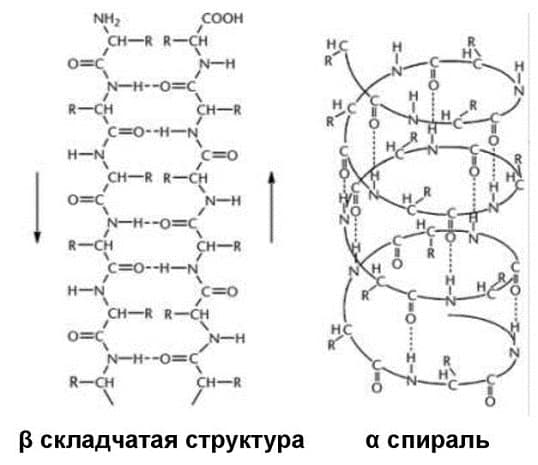
Вторичная структура белка
Свёрнутая в спираль одна или 2 полипептидные цепи образуют вторичную структуру. Её поддерживают водородные связи.
Большинство белковых молекул имеют вторичный уровень.
Третичная структура белка
Упаковка вторичной структуры в клубок образует третичный уровень организации.

Поддерживают данную структуру дисульфидные, солевые, сложноэфирные мостики, силы электростатического взаимодействия.
Четвертичная структура белка
Некоторые белковые единицы формируют сложные агрегаты в пространстве. Несколько упакованных в клубок белков, ориентированных относительно друг друга, создают четвертичную структуру.
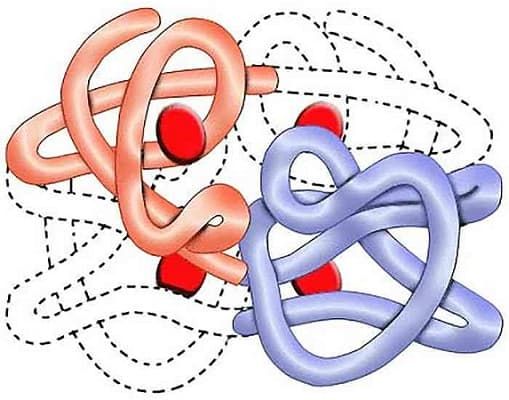
Удерживаются такие агрегаты водородными связями, электростатическими и прочими взаимодействиями.
Денатурация и ренатурация белка
Природные соединения проявляют разные свойства. Одно из важнейших свойств – денатурация белка. Это разрушение пространственной организации белковых молекул. Последовательность соединения аминокислот, а значит и химический состав, не изменяется.

Пространственная конфигурация может разрушаться в результате действия разных факторов:
-
высокой температуры;
-
радиации;
-
солей тяжёлых металлов;
-
щелочей;
-
кислот;
-
механических и иных факторов.
Если первичный уровень организации белка не нарушен, может идти обратная реакция – ренатурация. Это восстановление пространственного строения молекулы. Не все природные полимеры способны к восстановлению пространственной организации.
Иногда денатурация протекает необратимо, хотя первичная структура не разрушается. Функции белки способны выполнять, находясь в определенной пространственной конфигурации.
Протеины – простые белки
К простым белкам относят высокомолекулярные соединения, состоящие только из остатков аминокислот. В них содержатся незаменимые и заменимые аминокислоты.

Протеины применяются в спортивной среде для восполнения белковой массы в организме. Используют протеиновый порошок для приготовления коктейля, в качестве добавки к пище.
Протеиновый порошок получают в результате переработки продуктов животного происхождения: молока, мяса, яиц, рыбы. Организм будет получать протеины, если просто употреблять в пищу указанные продукты. Усвоение их будет идти медленнее.
Протеиды – сложные белки
Сложными называют белки, содержащие небелковые по природе вещества. Так называемые простетические группы.
В соответствии с химическим составом и наличием групп их классифицируют:
-
на нуклеопротеиды;
-
хромопротеиды;
-
липопротеиды;
-
гликопротеиды и другие.
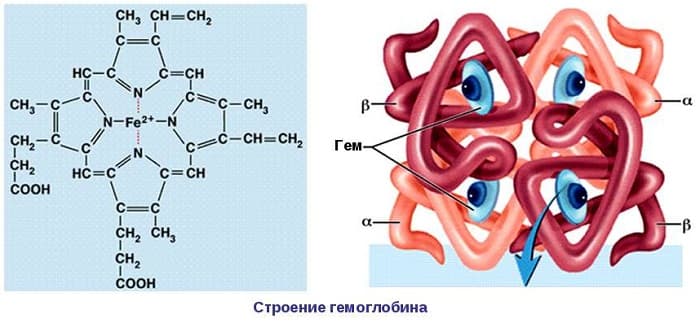
В состав протеидов входят элементы: магний, железо, медь и другие. Примером протеидов являются гемоглобин и миоглобин. Они выполняют важнейшие функции, принимают участие в обменных процессах.
Функции белков
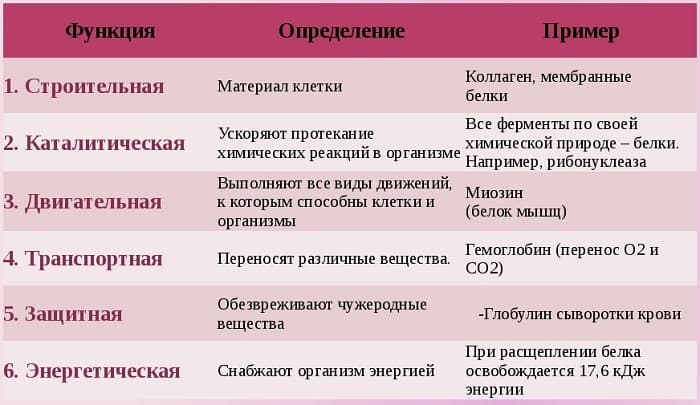
Белки выполняют в клетках организмов важные функции:
-
каталитические;
-
регуляторные;
-
структурные;
-
двигательные;
-
транспортные;
-
защитные;
-
запасные и другие.
Пространственная конфигурация белка оказывает существенное влияние на возможность выполнения функций.
