В данной статье мы расскажем вам о многочисленных химических свойствах такого органического вещества, как этилен. Во всех подробностях разберем химические реакции с этим веществом. Помимо химических свойств обязательно рассмотрим и общее строение этилена, а также применение данного алкена, основанное на его качествах и способностях.
Характеристики этилена
Этилен, или этен, имеет структурную формулу C2H4 и является простейшим представителем непредельных этиленовых углеводородов:
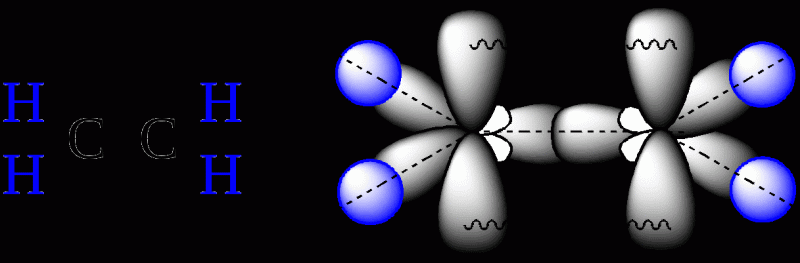
Рис. 1. Строение молекулы этилена
Важно! В молекуле этилена невозможно свободное вращение sp2-гибридизованных углеродных атомов друг относительно друга без разрыва пи-связи.
В обычных условиях данное органическое вещество является газом без цвета и запаха. А теперь можем перейти к главной теме — химическим свойствам этилена.
Главные химические свойства C2H4
Изучение химических способностей этена будет разделено на отдельные блоки, в которых четко и детально будут расписаны подробности взаимодействий.
Реакции присоединения
Если для предельных органических соединений характерны реакции замещения, то для алкенов, в частности этилена, типичны реакции присоединения:
- Гидрогалогенирование — присоединение галогеноводородов. Этилен взаимодействует с бромоводородом без особых условий, в результате чего получается бромэтан. Помните, что при присоединении реагента к несимметричному алкену действует правило Марковникова. Оно гласит о том, что атом водорода присоединяется к более гидрогенизированному углеродному атому, а галоген — к менее гидрогенизированному C.
- Гидратация — присоединение H2O. C2H4 реагирует с водой в присутствии концентрированной серной кислоты и при температуре. Продуктом реакции является этанол — одноатомный первичный спирт. Катализатором в данном случае может быть и фосфорная кислота. Если бы мы проводили аналогичное взаимодействие с пропеном, то получили бы пропанол-2 — вторичный спирт.
- Галогенирование — присоединение галогенов. В ходе этой реакции этен реагирует с хлором. Хлор присоединяется к C2H4, разрывая двойную связь, и на выходе получим 1,2-дихлорэтан. Реакция галогенирования является качественной на кратную связь.
- Гидрирование или дегидрирование — присоединение или отщепление атомов водорода. При гидрировании этилен взаимодействует с водородом в присутствии никелевого катализатора и температуры, образуя алкан — этан.

Рис. 2. Химические свойства этилена В случае дегидрирования при аналогичных условиях будут получаться водород и алкин — этин или ацетилен.
Реакция полимеризации
Полимеризация — это процесс соединения одинаковых простых молекул — мономеров, в более сложные — полимеры. Берется неограниченное количество молекул этилена, и при повышенных давлении и температуре, в присутствии катализатора образуется полиэтилен.
Важно! Обратите внимание, что в полиэтилене уже нет кратной связи, она разрывается в процессе реакции.
Реакции окисления
- Реакция Вагнера (в нейтральной среде) — окисление перманганатом калия в водной среде. Три молекулы этена реагируют с двумя молекулами перманганата и четырьмя H2O. В результате этого взаимодействия мы получим три молекулы этиленгликоля — двухатомного спирта. Также выделится гидроксид калия и два оксида марганца (IV). Единственным условием данной реакции может являться холодная среда, то есть наличие температуры в 0 градусов, но это можно и не указывать.
- Реакция Вагнера (в кислотной среде) — окисление перманганатом калия в среде, где находится серная кислота. Этен аналогично реагирует с перманганатом, но вместо воды в этот раз присутствует серная кислота. Соответственно — продукты реакции будут другие. Мы получим две молекулы углекислого газа, сульфаты марганца и калия, а также воду. Взаимодействие идет при термическом воздействии.
- Горение — алкены горят так же, как и все органические соединения. Этилен не является исключением. При сгорании этена образуются углекислый газ и вода. Так как данная реакция является экзотермической, то происходит выделение энергии.
- Обесцвечивание окраски бромной воды — данная реакция является качественной на наличие кратной связи. Важно то, что нельзя отличить, тройная это связь или двойная. Этен реагирует с раствором брома без каких-либо условий. В ходе взаимодействия образуется 1,2-дибромэтан. Исходная темная окраска исчезает, а остается прозрачная жидкость.
Реакция изомеризации
Данная реакция не может протекать с этиленом, потому что у него не существует изомеров.
Механизм реакции электрофильного замещения
Мы уже рассмотрели реакцию присоединения галогена к этилену. Но стоит отдельно рассказать о механизме данной реакции, который необходимо знать. В результате отталкивания от пи-связи этена в молекуле хлора происходит поляризация, благодаря которой один атом хлора становится частично положительно заряженным, а другой — частично отрицательно заряженным. Это приводит к смещению пи-связи и образованию пи-комплекса.

Рис. 3. Главные химические свойства этилена Из-за сильной поляризации в молекуле хлора происходит гетеролитический разрыв ковалентной связи. Положительно заряженный ион хлора присоединяется к углеродному атому. Второй атом углерода становится положительно заряженным. Происходит образование сигма-комплекса или карбокатиона. Отрицательно заряженный ион хлора присоединяется к положительному углероду. Образовался 1,2-дихлорэтан.
Применение этилена
Почему мы выделяем этот вопрос при изучении химических свойств этилена? Потому что применение данного органического вещества основано на всех его химических свойствах:
- В первую очередь, из-за своих многочисленных химических способностей алкены, в том числе и этилен, являются крайне ценным сырьем в химической промышленности.
- Этилен наряду с другими алкенами используют для ускорения созревания плодов и фруктов.
- C2H4 применяется в получение таких органических веществ, как этиловый спирт, этиленгликоль, дихлорэтан и т.д.
- Широко распространен в медицине, технике, парфюмерии.
- Благодаря реакциям полимеризации с участием этилена, образуется полиэтилен — очень полезное вещество с уникальными свойствами.
- Получение антифризов также связано с химическими свойствами этилена.
Благодаря этой статье, вы изучили и подробно рассмотрели все химические реакции, которые характерны для этилена — простейшего представителя алкенов. Перед этим кратко узнали о строении этого органического соединения, что позволило более четко взглянуть на его химическую активность в различных взаимодействиях. Мы оценили важность и пользу этена, а также его необходимость в современной жизни человека. Чтобы закрепить изученный материал, рекомендуем вам пройти тест, расположенный ниже и посмотреть познавательное видео.
